为落实《医疗器械注册与备案管理办法》《医疗器械临床试验机构监督检查办法(试行)》等相关要求,加强医疗器械临床试验机构监督管理,国家药品监督管理局食品药品审核查验中心组织制定了《医疗器械临床试验机构监督检查要点及判定原则(试行)》,经国家药品监督管理局同意,自2024年10月1日起施行。
一、起草背景
随着医疗器械产业的蓬勃发展及新品的层出不穷,临床试验的标准与要求亦随之提升,愈发凸显出构建严谨且系统性的监管架构的重要性,以确保医疗器械既安全又高效。《医疗器械临床试验机构监督检查要点及判定原则(试行)》(以下简称为“文件”)的出台,为临床试验实践提供了一份详实的操作蓝本,旨在统一并提升临床试验的执行标准,有效遏制潜在的违规操作,增强监管针对性和效率,确保问题及时发现与纠正,提升监管质量与效果。
二、主要内容

一
监督检查范围界定
? 机构与研究人员资质:机构资质检查包括机构的合法注册、备案状态以及开展特定类型医疗器械临床试验的能力和条件等。研究人员资质检查包括研究员的专业技能、培训记录、伦理教育情况及其对试验方案的执行能力等。
? 组织结构与管理体系:检查机构的组织架构是否合理,管理制度是否健全,包括质量管理体系、风险管理机制、应急处理预案等。
? 伦理审查委员会:评估伦理审查委员会的组成、运行情况,审查流程是否符合伦理审查的国家标准和国际原则。
? 试验设计与执行:确认临床试验方案的科学性、合理性,检查试验执行过程中的数据收集、记录、存储和分析是否规范。
? 受试者保护:检查知情同意书的内容、获取过程的合法性,对受试者隐私、安全的保护措施是否到位,不良事件报告和处理流程的建立与执行情况。
? 设施设备与材料管理:评估试验现场的硬件设施、仪器设备的校准与维护记录,以及试验用医疗器械的储存、分发、回收与处置是否符合要求。
? 文档记录与存档:检查试验相关的文件资料是否完整、真实、可追溯,包括试验方案、原始数据、统计报告、会议记录等。
二
判定原则
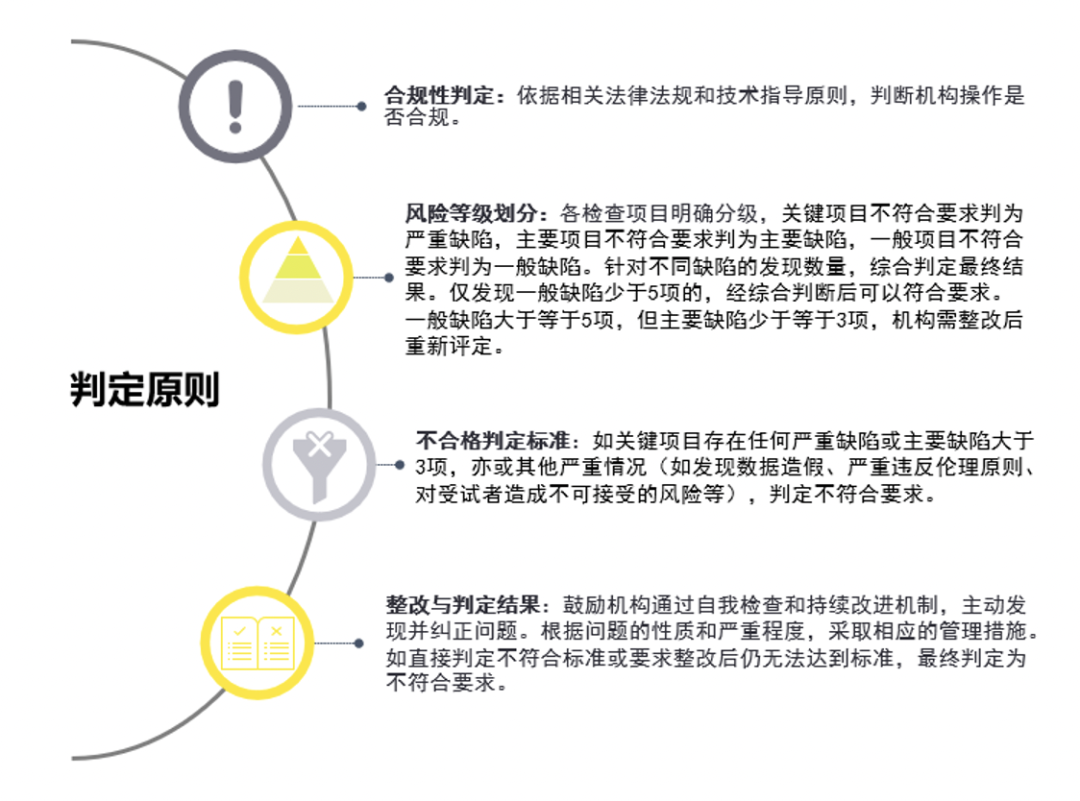
三
实施与执行
? 现场检查与文档审核:通过现场访问、文件审阅、人员访谈等方式,全面检查机构的实际情况。
? 问题发现与反馈:记录发现的问题,及时向机构反馈,要求制定并执行整改措施。
? 跟踪与验证:对机构的整改情况进行跟踪,必要时进行复核,验证整改效果。
三、行业影响
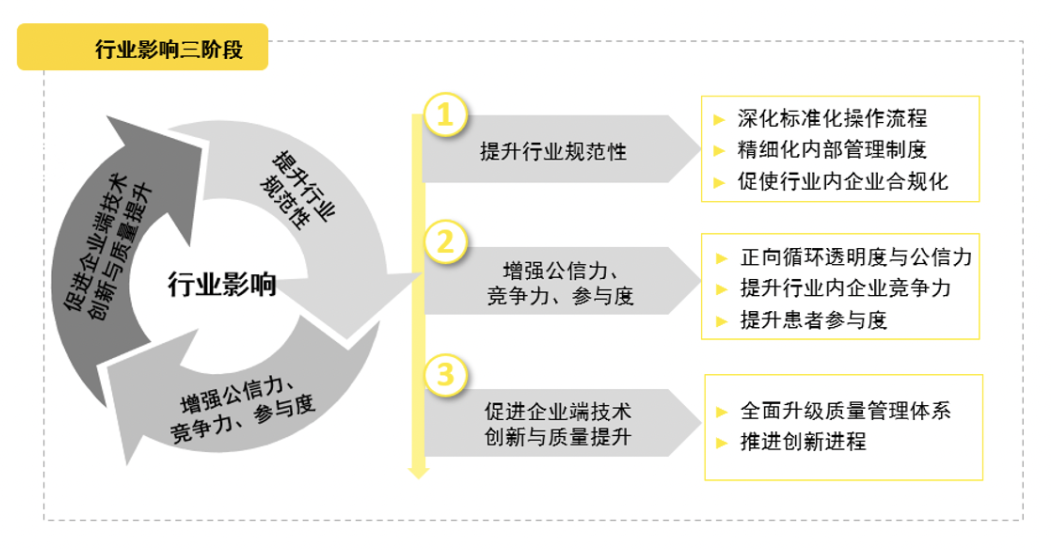
一
提升行业规范性
? 深化标准化操作流程:文件明确了临床试验标准流程和检查点,促进规范流程的普及与深化执行,加强日常运营合规性,推动行业向统一、高效的模式发展,利于最佳实践共享。
? 精细化内部管理制度:文件将促使企业细化内部制度,采用先进质量管理工具,确保操作的可追溯性和高效性,提升管理精度。
? 促使行业内企业合规化:规范性提升促使企业从被动遵守转为主动践行,将合规融入企业文化、战略及日常运营,作为核心竞争力,持续促进行业健康发展。
二
增强公信力、竞争力、参与度
? 正向循环透明度与公信力:通过监督检查结果的处理和一定程度内的结果公开,增强了公众、投资者以及科研界的信任。透明化的监管将提高行业信誉,有助于吸引更多的投资和参与,促进医学创新。
? 提升行业内企业竞争力:积极响应文件的企业将树立高标准形象,成为行业标杆,提升品牌影响力和市场占有率。透明度与合规性将增强消费者信心,扩大产品需求,稳固客户群。
? 提升患者参与度:随着临床试验的透明度和公信力增强,患者参与意愿的提升将进一步加速新医疗器械的研发进程。
三
促进企业端技术创新与质量提升
? 全面升级质量管理体系:文件强调质量优先,迫使企业重新审视和优化其质量管理体系。企业可能会采用更先进的质量管理模式(如数字化质量管理平台)实现质量数据的实时监控和快速响应。
? 推进创新进程:明确的监管指导将使企业打消对监管标准不明确的顾虑,帮助企业集中精力于研发创新和质量控制。在规范体系内,依托创新技术和产品,促进行业整体技术革新,提升竞争地位。
四、未来展望
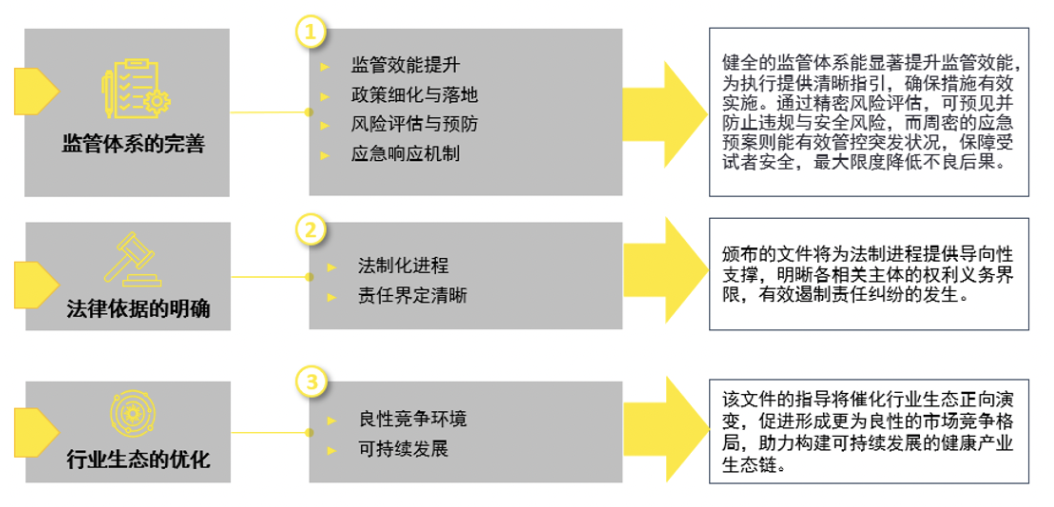
五、结束语
近年来,药品与医疗器械领域的合规监管政策及官方指导文件呈现出持续颁布的趋势,对相关医药企业提出了新的挑战。鉴于行业内政策环境的不断快速变化,企业需积极应对,对自身供应链及供应商与合作公司,在合规管理方面实施动态且有效的控制策略更新。此举旨在预先建立坚固的防御壁垒,以抵御由政策调整可能引发的合规风险,确保企业的运营活动始终与最新的监管要求保持高度契合。
安永咨询在医药合规领域积累了深厚的专业知识与广泛实践经验。我们的精英团队热忱期望与医药行业各界企业共享宝贵的合规管理洞见与成功案例,促进更多互惠互利的合作机会,携手实现共同繁荣与发展。


